Cómo reconocer y nombrar a los Hidróxidos y Oxácidos
- quimicafacil123
- 10 may 2018
- 1 Min. de lectura
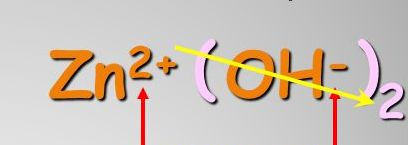
En el caso de los hidróxidos es muy simple por cuanto la cantidad de OH- que tiene coincide con el número de oxidación del metal. Una vez que se haya identificado éste, se le da el nombre con la nomenclatura elegida.
Ejemplos
Pb (OH)2: hidróxido plumboso (2 es el menor número de oxidación), hidróxido de plomo (II) o dihidróxido de plomo.
Fe (OH)3 : hidróxido férrico (3 es el mayor número de oxidación del hierro), hidróxido de hierro (III) o trihidróxido de hierro)
Oxácidos
Se los reconoce porque tienen la siguiente fórmula general:
HxNOy
Se ordena según electronegatividad creciente, primero el hidrógeno, luego el no metal y por último el oxígeno.
Para nombrarlos es necesario determinar cual es el número de oxidación del no metal. Para ellos se tiene en cuenta que la suma total debe ser 0 y que el hidrógeno tiene +1 y el oxígeno -2.
Ejemplo:
H2SO4 : 2. (+1) + S + 4.(-2) = 0
S = -2 + 8 = 6
Como 6 es el mayor número de oxidación del azufre se trata del ácido sulfúrico según la nomenclatura tradicional.
Entradas recientes
Ver todoÓxidos, hidruros, oxácidos, hidróxidos, oxisales, sales haloideas, sales ácidas, ácidos meta, orto y piro. Formulación, nomenclatura. Reacci

